Аналитический контроль является одной из ключевых стадий процессов очистки воды и водоподготовки, будь то очистка сточных вод или получение очищенной воды для нужд энергетики. Развитие процессов водоочистки и водоподготовки связано с применением все большего круга химических реагентов. При этом применение любого вещества требует наличия адекватных методов его аналитического определения.
Полиалкилгуанидины (ПАГ) - высокоэффективные биоцидные средства нового поколения [1]. Активные попытки внедрения ПАГ в процессы водоподготовки и обеззараживания сточных вод тормозятся отсутствием методов химико-аналитического определения данного класса препаратов. Ситуация осложнена тем, что ПАГ не образуют нерастворимых осадков, они оптически прозрачны, что делает их фотометрический анализ невозможным. ПАГ - полимеры малой молекулярной массы и, как остальные полимеры, обладают молекулярно-массовым распределением, что делает метод ионной хроматографии малоэффективным для их определения. За рубежом широкое применение получили препараты на основе дигуанидинов, которые, в отличие от ПАГ, за счет малого размера молекулы легко проникают сквозь клеточные мембраны, а далее в кровь человека, вызывая аллергические реакции. Кожа представляет для полимерных ПАГ непреодолимое препятствие.
При растворении в воде ПАГ диссоциируют на поликатионы и соответствующие им противоионы, которым часто является хлорид-ион. Гуанидин, один из исходных компонентов синтеза ПАГ, является сильным основанием. Гуанидиновые фрагменты в составе ПАГ имеют положительный заряд и являются катионными центрами.
Рис. 1 дает представление о принципе антисептического действия ПАГ.
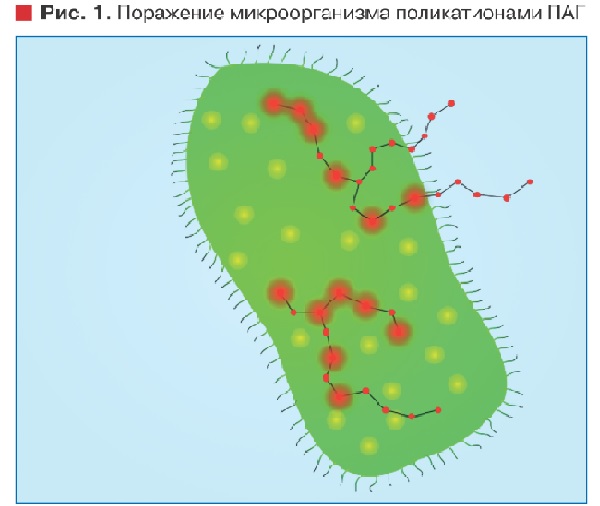
На клеточных стенах микроорганизмов присутствует большое количество анионных центров (представлены на рисунке желтым цветом). Поликатионы при контакте с клеточными стенками микроорганизмов необратимо блокируют присутствующие на них анионные центры (пораженные центры представлены красными пятнами). Это нарушает жизнедеятельность микроорганизмов и ведет к их гибели. В отличие от других антисептических средств, действие которых основано на блокировании анионных центров бактерий, каждый поликатион ПАГ способен поразить множество анионных центров, что повышает эффективность препаратов на их основе.
Вольтамперометрия на границе раздела фаз электролит-электролит является сравнительно новым методом в электроаналитической химии. В определенных условиях граница раздела фаз типа вода-нитробензол ведет себя как поляризуемый электрод, и с помощью четырехэлектродного потенциостата (в нашем случае «Экотест-ВА-4») можно управлять межфазной разностью потенциалов на указанной границе раздела фаз и фиксировать точки, соответствующие межфазному переходу ионов каждого вида. При этом каждый ион может быть охарактеризован своей межфазной неэлектростатической работой межфазного перехода и, соответственно, своим характерным потенциалом межфазного перехода.
Необходимым условием аналитического применения указанного метода является то, чтобы потенциал перехода искомого иона лежал в пределах поляризуемости границы раздела фаз электролит- электролит. При этом часто органическую фазу иммобилизируют в виде органического геля и помещают в специальный корпус. Полученные таким образом датчики называют амперометрическими ионоселективными электродами [2]. Пока они находят применение в лабораторной практике на уровне исследований, однако можно ожидать их массового использования. На рис. 2 представлено рабочее место для выполнения измерений на границе раздела фаз электролит- электролит.

Измерения проводили при помощи вольтамперометрического анализатора (1) «Экотест-ВА-4», подключаемого по четырехэлектродной схеме в электрохимической ячейке (2). Управление вольтамперометрического анализатора осуществляется при помощи персонального компьютера (3).
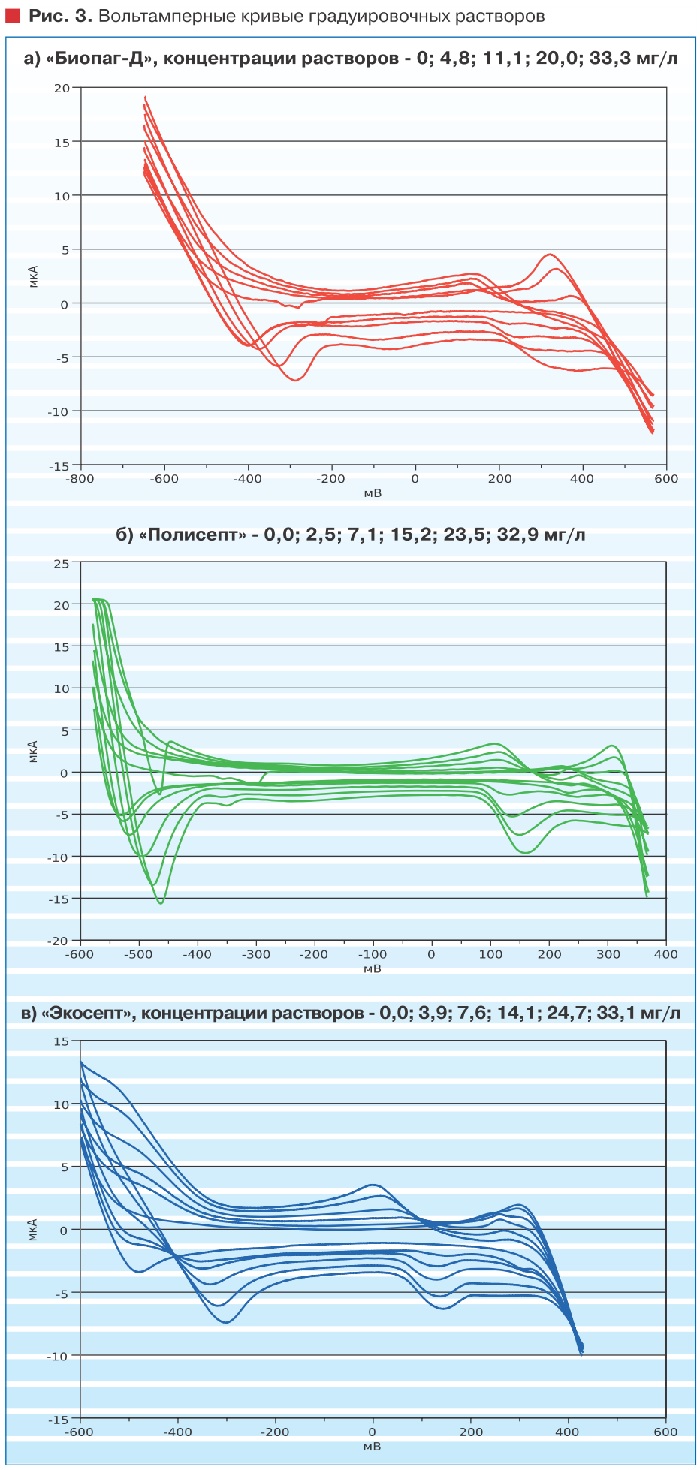
Аналитический сигнал ПАГ нам впервые удалось получить на разработанных фирмой «Эконикс-Эксперт» датчиках. Сигнал отчетливо виден на измеряемых вольтамперных кривых, измеряемых методом постояннотоковой вольтамперометрии на границе раздела фаз электролит-электролит. На рис. 3 представлены вольтамперные кривые растворов препаратов «Биопаг-Д», «Экосепт» и «Полисепт». Аналитические сигналы находятся на нижних кривых в области потенциалов от +150 до +300 мВ.
Электрохимическая ячейка состоит из двух полуэлементов - органического и водного, представляющих собой растворы не смешивающихся электролитов, в каждый из которых погружены электрод сравнения и вспомогательный электрод. Наблюдаемый на вольтамперных кривых ток - ток, проходящий через границу раздела двух полуэлементов, а напряжение - разность потенциалов между фазами [3].
Перед каждым измерением в ячейке заменяют органический электролит, вносят пробу в электрохимическую ячейку и добавляют фоновый электролит (0,01-молярный раствор MgSO4).
На рис. 4 представлены соответствующие градуировочные графики, построенные по результатам анализов данных.
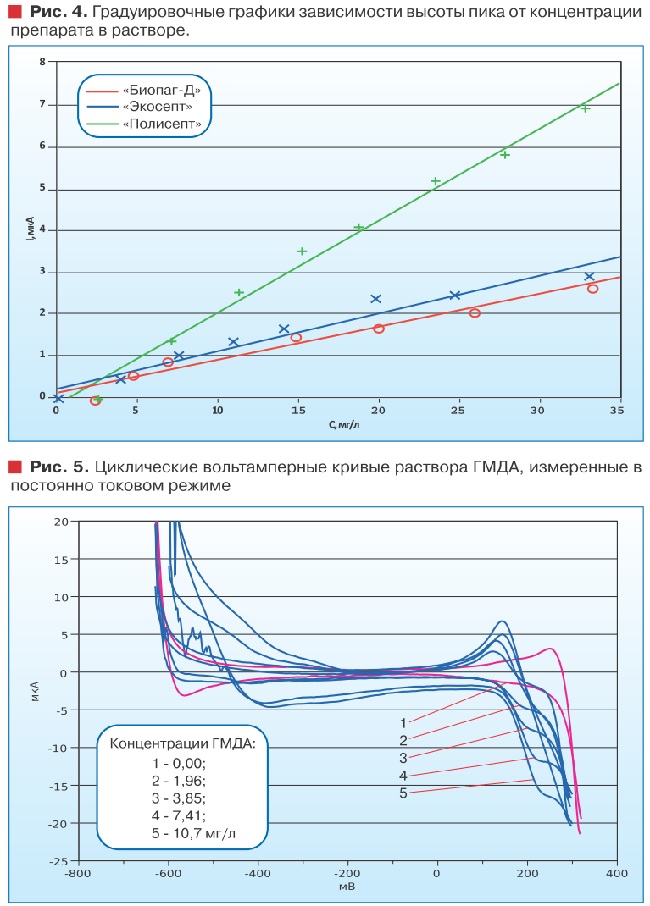
Показатель R2 для градуировки препарата «Биопаг-Д» - 0,944, «Полисепт» - 0,991 и 0,947 для препарата «Экосепт». Отклик системы на добавки «Полисепта» сильнее, чем для «Биопага» и «Экосепта», примерно в два раза. Как видно из рис. 3, на вольтамперных кривых растворов ПАГ всех трех марок при низких концентрациях (ниже 5 мг/л) наблюдается побочный пик, который с повышением концентрации препарата в растворе поглощается основным аналитическим сигналом. Для препарата «Биопаг-Д» побочный пик проявляется примерно при 300 мВ, для «Экосепт» значение потенциала пика составило также около 300 мВ, пик побочного сигнала «Полисепта» проявился при 250 мВ. Первоначально возникло предположение, что побочный сигнал - это пик не прореагировавшего в процессе синтеза препарата мономера. Результаты последних исследований растворов гексаметилендиамина (ГДМА), одного из исходных веществ при синтезе ПАГ, подтвердили это предположение.
На рис. 5 представлены циклические вольтамперные кривые гексаметилендиамина гидрохлорида - одного из применяемых при синтезе ПАГ исходных мономеров.
Как видно из представленных вольтамперограмм, сигнал гексаметилендиамина, а точнее сигнал межфазного перехода его катиона, наблюдается при потенциале +250 мВ, он находится почти на границе диапазона рабочих потенциалов. Это является убедительным доказательством того, что побочный сигнал, наблюдаемый при анализе ПАГ, есть ничто иное, как сигнал не прореагировавшего мономера.
Сигналы ионов распределяются на вольтамперных кривых по степени гидрофобности: гидрофобные - к центру, гидрофильные - по краям. В полимере на одну гидрофобную гексаметиленовую цепочку приходится один гидрофильный гуанидиновый фрагмент; в мономере на одну гексаметиленовую цепочку приходятся два гуанидиновых фрагмента. Это делает мономер более гидрофильным, что объясняет положение его сигнала на шкале потенциалов - он находится ближе к границам рабочих потенциалов.
Несмотря на полимерную структуру данных препаратов [4], как видно из рис. 3, для всех трех препаратов входу поликатионов в органическую фазу и выходу из органической фазы соответствует одиночный сигнал. Поскольку результаты измерений для различных ПАГ совпали, по-видимому, соответствующий потенциал перехода определяется природой гесаметиленгуанидинового фрагмента, а не структурой молекулы ПАГ и его молекулярной массой. Это, в отличие от хроматографических методов, которые разделяют сигналы изомеров, позволяет определять суммарную массовую концентрацию препарата.
Таким образом, вольтамперометрия на границе раздела фаз электролит-электролит идеально подходит в качестве метода оперативного контроля содержания ПАГ в водных растворах.
На данный момент основным препятствием для внедрения данного метода анализа является недостаточно высокая чувствительность метода. Сейчас она составляет около 1 мг/л. Так как ПДК для ПАГ составляет 0,1 мг/л, разрабатываемая методика должна позволять концентрации ПАГ от 0,05 мг/л. Эта проблема может быть преодолена применением инверсионного режима вольтамперометрических измерений. Данный режим позволяет достигать минимально определяемых концентраций порядка сотых миллиграмма на литр в случае перхлорат-ионов и перренат-ионов. Другим возможным решением проблемы может быть безреагентное концентрирование пробы. Успех последнего метода позволяет предполагать, что таким образом можно существенно повысить чувствительность метода (более чем на два порядка).
Задача контроля состава средств на основе ПАГ уже может быть решена с применением вольтамперометрии на границе раздела фаз электролит- электролит. Концентрация ПАГ в средствах на их основе требует контроля, который затруднителен или невозможен существующими методами. Зачастую концентрация ПАГ в препаратах на их основе составляет 20-50%. Для анализа таких объектов необходимо предварительно разбавлять пробу до удобных для определения на данном этапе 4-6 мг/л.
Анализ препаратов на основе ПАГ показал, что методика с применением вольтамперометрии на границе раздела фаз электролит-электролит дает надежные результаты. На рис. 5 представлены вольтамперные кривые, измеренные при определении полигексаметиленгуанидина (ПГМГ) в препарате «Дезавид».
Перед анализом исследуемый препарат был разбавлен в 10 000 раз. Измерение и обработка вольтамперных кривых проводились с применением программного обеспечения «Экотест- ВА» второго поколения. Полученное при помощи программы значение концентрации ПГМГ после пересчета из- за разбавления пробы (4 мл исследуемого раствора были добавлены в 20 мл фонового электролита) и самого «Дезавида» в 10 000 раз составило 328 г/л. Полученное значение концентрации отличается от заявленных производителем 45% масс. на 27%. Такое значение относительной погрешности сопоставимо с погрешностью вольтамперометрии на твердотельных электродах, которая позволяет достигать точности порядка 20-30%.
В состав препарата «Дезавид» помимо ПГМГ входит и алкилдиметил- бензиламмоний хлорид. Как видно из рис. 6, на вольтамперных кривых разбавленного раствора препарата при потенциале минус 300 мВ наблюдается сигнал, не наблюдаемый на представленных ранее вольтамперных кривых. На основании исследований растворов чистого алкилдиметилбензиламмония хлорида его сигнал был опознан.
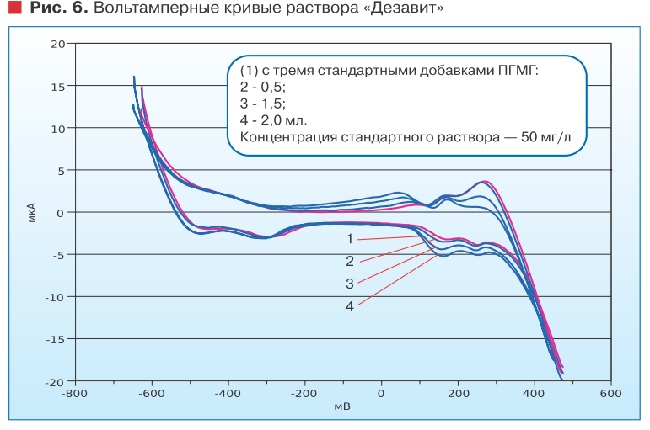
Приведенный пример анализа растворов «Дезавид» демонстрирует возможность применения вольтамперометрии на границе раздела фаз электролит-электролит для определения количественного и качественного состава препаратов на основе ПАГ. Проблема чувствительности в данном случае отсутствует.
Активно проводимые в настоящее время исследования позволяют рассчитывать на распространение метода вольтамперометрии на границе раздела фаз при анализе препаратов на основе ПАГ. В существующем виде метод уже может применяться для контроля состава ПАГ и препаратов на их основе. Следующими шагами по внедрению метода в производство должны стать, во-первых, метрологическая аттестация методик контроля состава препаратов на основе ПАГ, во-вторых, разработка и аттестация более чувствительной методики измерения концентрации ПАГ в воде при очистке и обеззараживании воды.
Вольтамперометрический анализ на границе раздела двух нерастворимых электролитов позволяет существенно расширить возможности современной аналитической химии. Особенно интересной представляется возможность анализа таких неординарных объектов как полиалкилгуанидины, перспектива применения которых выглядит заманчивой альтернативой хлорирования воды при ее очистке [5].
Существенным преимуществом метода при этом являются не только простота оборудования и его освоения, что особенно актуально для контроля качества воды в водоочистке и водоподготовке. Дополнительный его плюс - дешевизна по сравнению со сложными хроматографическими системами, применяемыми иногда для решения аналогичных задач.
Кратко опишем другие подходы к аналитическому определению ПАГ.
Бактерицидные средства на основе ПАГ находят все возрастающее применение в медицине, косметологии, разнообразных отраслях экономики, в быту. Наиболее распространенными на отечественном рынке являются препараты этой группы под названием «Биопаг», «Полисепт», «Экосепт». В отличие от зарубежных аналогов, представляющих собою дигуанидины (например, хлоргексидин), полигуанидины плохо проникают через кожу и слизистые оболочки в кровь, и, соответственно, являются более гипоаллергенными. Кроме того, поскольку полимерные катионы поражают сразу большое количество анионных центров на бактериальных мембранах, они эффективнее, чем дигуанидины, по своей дезифицирующей способности.
Одним из факторов, ограничивающих применение полигуанидинов для обеззараживания больших объемов воды (например, сточных вод, воды в плавательных бассейнах), является отсутствие адекватных подходов к их химико-аналитическому определению. В то время как дигуанидины легко определяются методами ионной хроматографии, ПАГ с молекулярными массами 1500-5000 «Дальтон» достаточно трудно поддаются определению в низких концентрациях.
К настоящему моменту существует ряд подходов к определению указанных бактерицидов. Например, существует методика определения препаратов «Биопаг» и «Полисепт», представляющих ПАГ, методом фотоколориметрии в присутствии красителя «Эозина Н». При этом методика эмпирическая, оптическая плотность «Эозина Н» нелинейно возрастает от 1,5 до примерно 2, а затем убывает при увеличении концентрации препарата «Биопаг» от 1 до 50 мг/л. Методика не позволяет фиксировать концентрации полигуанидинов ниже 1 мг/л, а необходимо определять 0,05 мг/л, т.к. ПДК составляет 0,1 мг/л. Таким образом, химико-аналитическое определение ПАГ представляет собою техническую проблему, т.к. традиционные химико- аналитические методы лишь ограничено применимы.
Как видно из сказанного, предложенный подход имеет существенные преимущества по сравнению с имеющимися. Во-первых, он обеспечивает идентификацию биоцида по потенциалу перехода ионов, во-вторых, он более чувствительный, в третьих, он реализуется на недорогой отечественной аппаратуре.
Литература:
1. В.И. Голышевская, Л.П. Мартынова, А.Л. Тарновский, И.И. Воинцева. Перспективы использования полигуанидиновых препаратов для борьбы с туберкулезной инфекцией // Экологически безопасные полимерные биоциды. М.: 2000. Выпуск 1. С.32.
2. Н.К. Зайцев .Физико-химические основы переноса заряда через границу раздела фаз электролит-электролит и его приложения в аналитической химии. М.: РГУ нефти и газа им. И.М. Губкина. 2004. 431с.
3. С.В. Шорин. Исследование явления переноса ионов через границу раздела фаз электролит/электролит и его применение при анализе водных растворов. М.: РГУ нефти и газа им. И.М. Губкина. 2003. 167с.
4. С.А. Кедик, О.А. Бочарова, Ха Кам Ань, А.В. Панов, И.П. Седишев, Е.С. Жаворонок, Г.И. Тимофеева, В.В. Суслов, С.Г. Бексаев. Структура и молекулярно-массовые характеристики гидрохлоридов олигогексаметиленгуанидинов // Химико-фармацевтический журнал. Том 44, №10, 2010. С.40.
5. О.Ю. Кунецов, Н.И. Данилина. Обеззараживание природных и сточных вод без использования хлорсодержащих реагентов. // Экологически безопасные полимерные биоциды. М.: 2000. Выпуск 1. С.59.
Журнал «Вода Magazine», №3 (55), 2012 г.
