УДК 628.113+628.196
Ключевые слова: водоснабжение, коррозия, растворимость, дезинфекция, активный хлор, озон
Обеззараживание воды применяется для устранения из нее микроорганизмов и вирусов, из-за наличия которых вода становится непригодной для питья, хозяйственных нужд или промышленных целей. При этом одним из видов обеззараживания является дезинфекция, которая представляет собой комплекс мероприятий, направленных на уничтожение возбудителей инфекционных заболеваний и разрушение токсинов на объектах внешней среды.
В настоящее время наибольшее распространение получили методы обеззараживания и дезинфекции с применением сильных окислителей, таких как хлор, хлорная известь, гипохлорит натрия и кальция, озон. Также достаточно широкое применение на практике находит физический метод - УФ-обработка. В таблице 1 представлены результаты анализа применения различных способов обеззараживания и дезинфекции в различных странах [1].

Озон имеет высокий окислительно-восстановительный потенциал - 2,07 В (для сравнения: у Cl2 -1,36 В, у O2 - 1,23 В), что является главной причиной его активности по отношению к различного рода загрязнениям воды, включая микроорганизмы [2]. В отсутствие бромидов в обрабатываемой воде не образуется побочных продуктов [3]. В то же время озон более токсичное и коррозионно-активное вещество, но при этом для обеззараживания требуется в десятки раз меньшее время воздействия.
Зарубежный опыт применения методов обеззараживания воды показывает увеличение количества станций водоподготовки с применение озонирования в качестве одной из ступеней очистки воды. Так, на территории Европы и США действуют более 1200 водопроводных станций [4], применяющих озонирование как одну из ступеней технологического процесса очистки воды. Применение технологии озонирования воды за рубежом можно также выразить удельным показателем на душу населения, характеризующим количество водопроводных станций, на которых применяется озонирование. Данный показатель варьируется в достаточно широких пределах: от 0,39 и 0,64 в Японии и США соответственно до 13,8 в Швейцарии. Низкое значение данного показателя в Японии и США говорит о малом применении озонирования в этих странах и преимущественном использовании хлорирования на станциях водоподготовки [5].
При использовании хлорсодержащих веществ и озона в процессах водоподготовки необходимо обращать внимание на следующие важные вопросы:
- растворимость озона в воде;
- коррозионная активность дезинфицирующих растворов к материалам сетей и сооружений водоподготовки;
- эффективность инактивации микроорганизмов при использовании различных дезинфицирующих растворов в условиях эксплуатации;
- параметры обработки сетей и сооружений водоснабжения;
- воздействие на окружающую среду;
- технико-экономическое обоснование использования предлагаемых веществ и технологии.
Применение озона в водоподготовке осложнено в том числе относительно низкой растворимостью озона в воде в сравнении с хлорсодержащими веществами. Для увеличения растворимости необходимо применять специальные устройства, увеличивающие время контакта, площадь поверхности контакта, или обеспечивающие интенсивное перемешивание озона с водой. Как правило, озоно-воздушная смесь диспергируется и подается вводу в виде мелких пузырьков (0,1-1 мм).
В литературе присутствуют данные по растворимости озона в воде в зависимости от температуры по данным Хорватса [6], а также в справочнике растворимости Когана В. Б. [7], в котором используется коэффициент Бунзена. Названные источники позволяют теоретически спрогнозировать равновесную концентрацию озона при заданных условиях. Однако на растворение озона в природной воде влияет множество факторов, таких как наличие окисляемых веществ, концентрация озона в газовой смеси, давление, размер пузырьков газа, создаваемых аэратором и ряд других, которые в указанных формулах не учитываются. Так, в работе [8] приведены экспериментальны данные по изучению растворимости озона в слое воды глубиной до 4 м в зависимости от таких параметров обработки как время обработки, расход газовой смеси, концентрация озона в газовой смеси, высота слоя жидкости. Исследования проводились на установке, представленной на рис. 1.

По результатам экспериментальных исследований было получено регрессионное уравнение, описывающее концентрацию озона в воде (Сv мг/ дм3) от исследуемых параметров:
Cv = 3,9436 - 27,2356 • D + 0,0339 •
•Сг + 0,0286•T - 0,0456 • H + 0,0247•
•Q -155,3858 • D2 - 0,0003 • T2 +
+ 0,0522 • eн.
где Сv - концентрация озона в воде мг/дм3; D - диаметр колонны, м (D = 0,1-0,3 м); Сг - концентрация озона в газовой смеси, г/м3 (Сг = 2,7-55 г/м3); Т - время насыщения воды, мин (Т = 10-60 мин); Н - высота отбора пробы, м (Н = 0-4 м); Q - расход озоно-воздушной смеси, дм3/мин (Q = 3,3-700 дм3/мин).
Растворимость озона в воде, как и скорость его разложения, зависит от температуры, активной реакции среды и ее солевого состава. При понижении температуры и повышении рН растворимость озона возрастает, при этом основные соли снижают его растворимость, а нейтральные повышают [9]. Скорость же деструкции озона увеличивается при повышении температуры, рН и окисляемых веществ.
Необходимо отметить, что растворение озона в воде при различных значениях pH приводится во многих исследованиях [10-14], однако результаты кинетики распада озона достаточно сильно отличаются за счет различных условий проведение экспериментов. Так, установлено [15], что применяемые буферирующие добавки (фосфаты, борная кислота и др.) не индифферентны по отношению к озону и продуктам его распада. Они также могут взаимодействовать с гидроксильными радикалами, образующимися в процессе разложения озона в воде. В работе [16] приведен механизм цепной реакции взаимодействия озона с примесями, находящимися в воде. Что касается растворения озона в достаточно кислых средах, то исследования по данной теме свидетельствуют об увеличении реакционной способности озона [17]. Механизм взаимодействия озона с органическими соединениями в присутствии сверхкислот объясняется в предположении образования протонированного озона - интермедиата, обладающего очень сильными электрофильными свойствами [18, 19]. Известно, что молекула О3 в водных растворах реагирует с протонированными формами соединений намного медленнее, чем с депротонированными [20]. Поэтому специфический кислотный катализ реакций с участием озона объясняется в предположении образования именно протонированного озона, который обладает повышенной реакционной способностью по сравнению с обычным озоном [18].
Как показали исследования по определению кинетики разложения озона по высоте столба жидкости [21] (в эксперименте использовалась вода непосредственно из водозаборной скважины), около 96% его разлагается в течение 20 мин (рис. 2).

Одним из важных практических вопросов при использовании озона в процессах водоподготовки является сравнение его коррозионной активности с растворами хлорсодержащих веществ.
Сравнительный анализ коррозионной активности хлорсодержащих дезинфицирующих растворов, таких как гипохлорит натрия, гипохлорит кальция, хлорная известь, хлорамин с концентрациями по активному хлору 50, 100 и 150 мг/дм3, а также насыщенного раствора озона в воде проводился для углеродистых сталей марок Ст3, сталь 20 и сталь 15 [22, 23], а также образцов материалов обсадных труб водозаборных скважин, которые использовались при бурении скважин в 80-х-90-х годах, это образцы из углеродистой стали марок 08пс; 10; 10пс; 12мс; 14пс; 20; 45.
Исследования проводили весовым и косвенным электрохимическим методом - методом Зомельфельда. Определение группы стойкости металла по отношению к исследуемым растворам был определен через рассчитанные глубинный и весовой показатели коррозии. В указанных выше работах описаны физико-химические процессы, происходящие на поверхности металлов в обрабатываемых средах. Установлено, что наибольшей коррозионной активностью среди хлорсодержащих дезинфицирующих растворов обладает гипохлорит натрия, среди всех исследуемых растворов - насыщенный раствор озона в воде. Однако отмечено, что, например, в процессах дезинфекции сооружений водоснабжения благодаря значительно меньшему времени обработки озоном в сравнении с хлорсодержащими реагентами весовой показатель коррозии при использовании озона будет значительно меньше, чем минимальный весовой показатель коррозии при использовании хлорсодержащих реагентов.
Результаты изучения эффективности обеззараживания водопроводной воды хлорсодержащими реагентами показали, что при рекомендуемых СанПиН условиях обработки (6 часов при концентрациях активного хлора 50-100 мг/дм3) обеспечивалось 100% обеззараживание воды для всех исследованных тест-организмов из коллекции кафедры биотехнологии и биоэкологии БГТУ (г. Минск). Уменьшение времени воздействия до 0,5-1,5 час. привело к снижению эффективности обеззараживания гипохлоритом натрия воды, загрязненной бактериями E. coli, на 0,5-1%, тогда как эффективность воздействия хлорной известью сохранялась. Такие же закономерности наблюдались и при использовании хлорсодержащих дезинфицирующих веществ на бактериях Clostridium sp. и Pseudomonas fluorescens.
Результаты изучения эффективности дезинфекции озоном по исследуемым бактериям представлены в таблице 2 [21].
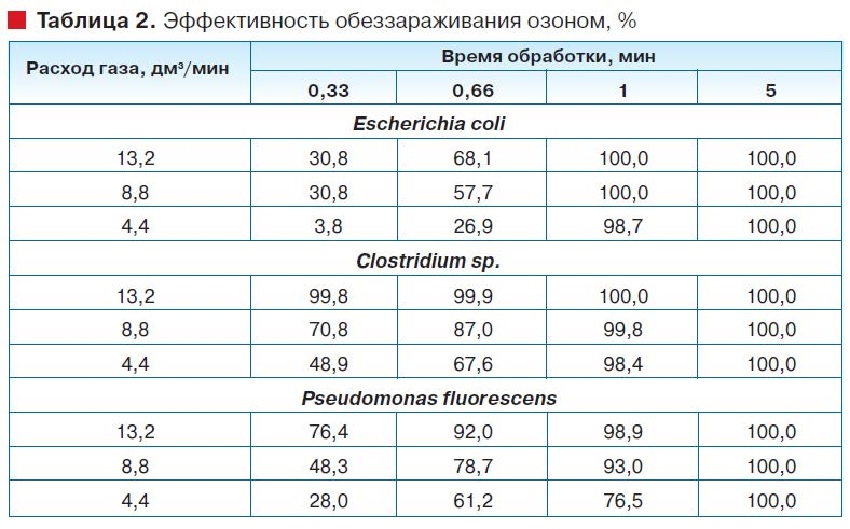
Из таблицы 2 видно, что оптимальное время обработки, необходимое для достижения 100% инактивации исследуемых микроорганизмов, составляет менее 5 мин.
Анализ эффективности дезинфекции исследуемых растворов проводили на металлических пластинках из стали Ст3, предварительно подвергнутых коррозии при воздействии хлорсодержащих дезинфицирующих средств в течение 12 часов, и бетонных образцах [24]. В качестве объекта исследования использовалось сообщество микроорганизмов, сформировавшееся на фильтре механической очистки воды из частной водопроводной скважины в течение полутора лет. В работе [24] отмечено, что эффективная дезинфекция при использовании хлорсодержащих дезинфектантов достигается при времени воздействия более 12 часов и концентрации активного хлора более 100 мг/дм3. Полное обеззараживание поверхностей из стали достигается при дозе озона 0,4 г и более, тогда как для бетонных поверхностей доза должна составлять более 0,8 г озона. При концентрации озона в воде более 2 мг/дм3 рекомендуемое время обработки должно составлять не менее 20 мин. В условиях проведенного эксперимента критерий СxТ для активного хлора в 2250-10800 раз больше, чем для озона [24].
В отличие от непрерывных процессов (окисление, обеззараживание) время обработки озоном в случае периодических процессов (дезинфекция) будет лимитироваться скоростью растворения озона в воде до достижения требуемой минимальной концентрации.
Для оценки и сравнения использования хлорсодержащих веществ и озона в процессах водоподготовки использовали методы анализа стоимости жизненного цикла и оценки воздействия на окружающую среду на этапах жизненного цикла. Анализ проводили на примере технологий дезинфекции сооружений водоснабжения [25].
На рис. 3 показана общая структура жизненного цикла рассматриваемых технологий, включающая стадии от добычи сырья до утилизации отработанных растворов.
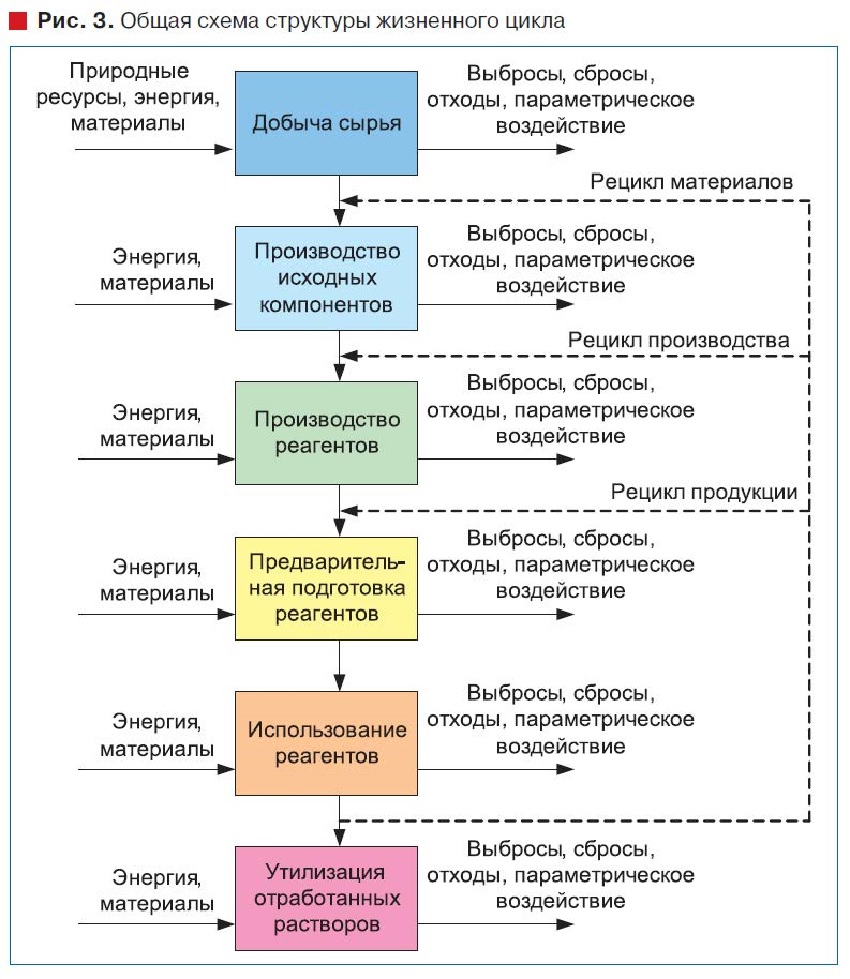
Воздействие на окружающую среду происходит на всех представленных этапах, как и совокупность различных затрат. Поскольку технологии дезинфекции являются потребителями готовых реагентов, то для оценки воздействия на окружающую среду рассмотрены этапы от получения реагентов, а при анализе стоимости жизненного цикла, от закупки оборудования и использования реагентов, до утилизации отработанных растворов.
Как следует из результатов проведенного инвентаризационного анализа, рассмотренные варианты применения различных веществ для дезинфекции сооружений водоснабжения характеризуются такими экологическими аспектами, как потребление
сырьевых материалов и энергии, а также выбросы загрязняющих веществ в атмосферный воздух, сбросы сточных вод в водные объекты или в местную сеть канализации, образование отходов.
Согласно этапам оценки воздействия жизненного цикла по имеющимся входным и выходным потокам установлены категории воздействия. На основании данных инвентаризационного анализа проводилась оценка значимости потенциальных воздействий исследуемой системы на окружающую среду [26]. Для оценки жизненного цикла процесса дезинфекции сооружений водоснабжения применялся программный продукт SimaPro 804, включающий метод исследования IMPACT 2002+ V2.12 / IMPACT 2002+.
Первоначально определялись категории воздействия (канцерогенные эффекты, респираторные эффекты, истощение озонного слоя, экотоксичность для водных и земельных ресурсов и др.). Результаты применения различных дезинфицирующих веществ по категориям воздействия представлены на рис. 4.
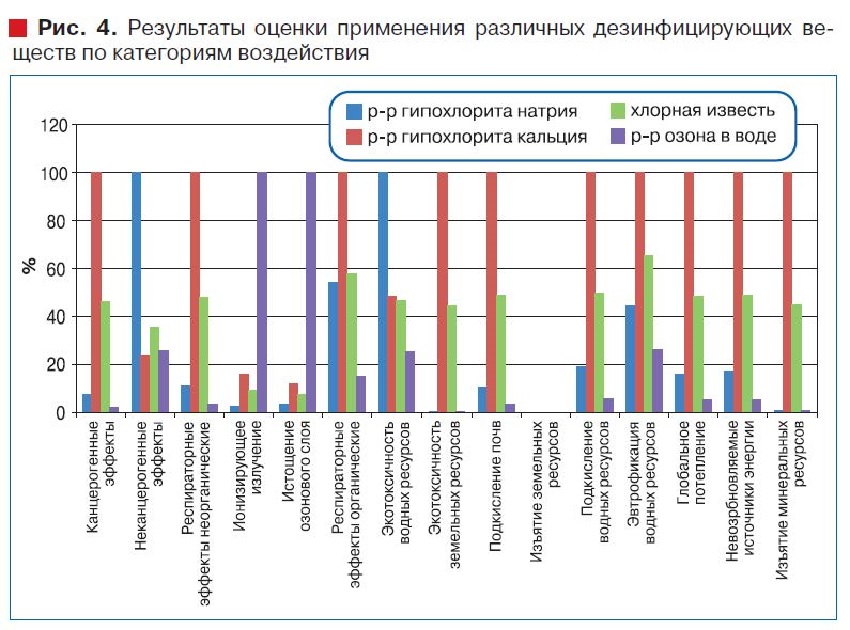
Из графика видно, что наиболее небезопасным хлор содержащим дезинфицирующим веществом для окружающей среды и человека является использование гипохлорита кальция.
Следующим этапом оценки жизненного цикла являлось взвешивание, заключающееся в оценке значимости каждой категории воздействия для объединения значений категорий в единую величину, отражающую экологическую характеристику исследуемой системы. Результаты ОЖЦ на данной стадии представлены на рис. 5.

Применение методики оценки жизненного цикла для сравнения применения различных веществ для дезинфекции сооружений водоснабжения показало, что наименьшее значение экоиндикатора соответствует варианту применения раствора озона в воде. Кроме того, необходимо отметить, что из вариантов применения хлорсодержащих веществ наилучшей характеристикой обладает гипохлорит натрия.
Оценка стоимости жизненного цикла приведена для стадии использования реагентов.
При расчете суммы текущих затрат учитывали:
- затраты на сырье и материалы;
- затраты на заработную плату;
- амортизационные отчисления;
- затраты на технологическую энергию;
- затраты на технический уход за оборудованием;
- затраты на текущий ремонт оборудования;
- затраты на содержание рабочей площади;
- затраты на перемещение установки к месту обработки.
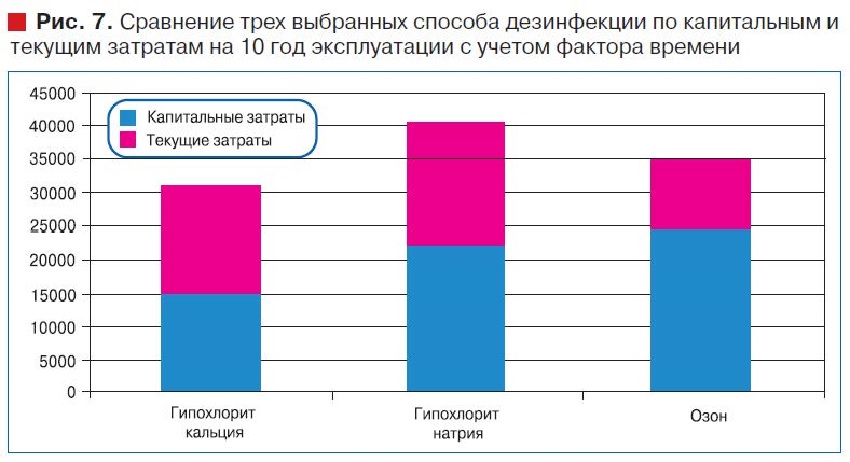
На рис. 6 и 7 представлены результаты сравнения трех выбранных способов дезинфекции по капитальным и текущим затратам без учета фактора времени (рис. 6) и с учетом фактора времени на 10 год эксплуатации установок (рис. 7).
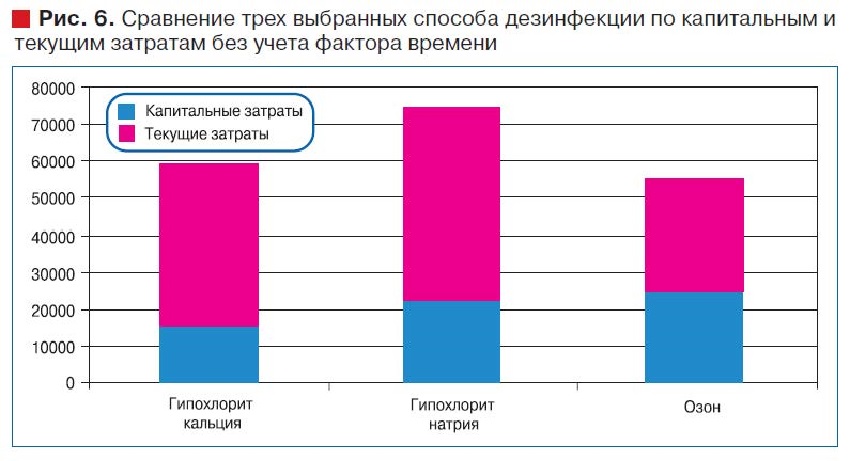
На рис. 8 представлено сравнение статей текущих затрат по каждому варианту дезинфицирующего вещества.
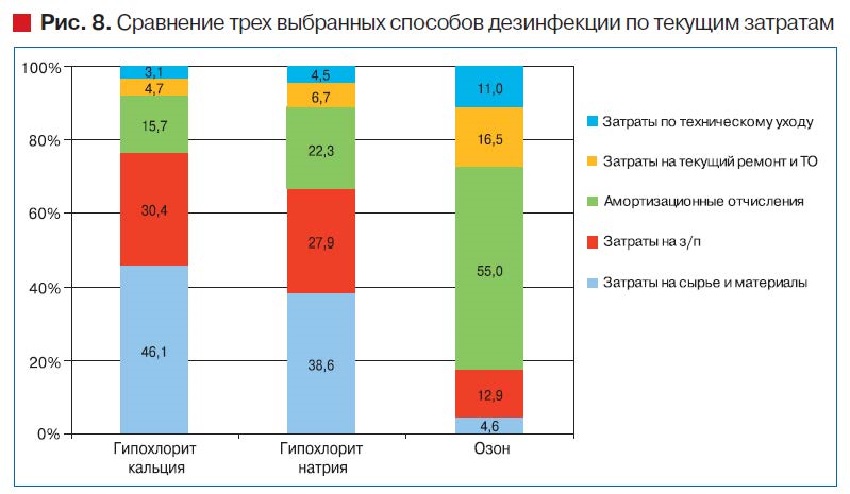
По результатам расчета технико-экономических показателей без учета фактора времени технология дезинфекции с использованием озона являются более экономически эффективной, чем при использовании хлорсодержащих дезинфицирующих растворов, а с учетом фактора времени является сопостовимой по совокупности затрат (капитальные вложения наибольшие, в то время как текщие затраты наименьшие). При этом наибольшую долю текущих затрат при использовании хлорсодержащих реагентов составляют затраты на сырье и материалы, а при использовании озона - амортизационные отчисления.
Заключение
Оценка жизненного цикла позволила определить количественные экологические показатели различных дезинфицирующих веществ, включая стадии их производства, приготовление реагента и непосредственно процесса дезинфекции. На основании оценки жизненного цикла можно предсказать возможные последствия по таким категориям воздействия как здоровье человека, состояние экосистем, а также истощение природных ресурсов, а также обосновать выбор наилучшей технологии при сравнении альтернативных вариантов.
Среди рассмотренных вариантов наиболее эффективным из хлорсодержащих реагентов является гипохлорит натрия. Однако если сравнивать хлорсодержащие реагенты с озоном, то технологии дезинфекции с использованием последнего являются наиболее эффективными.
Использование озона приводит к упрощению процесса, повышению эффективности дезинфекции, снижению времени обработки и, соответственно, времени простоя сооружений, меньшему коррозионному воздействию на металлические части скважины, а также можно отметить его экологическую безопасность. Применение озона для дезинфекции устраняет необходимость обезвреживания раствора после использования, как это происходит при дехлорировании, поскольку озон распадается на кислород в воде в течение небольшого периода времени.
Литература:
1. Leszczynski A. Ocena efektywnosci dezynfekcji studni glebinowych i rurociagow metoda ozonowania: praca dyplomowa magister- ska. Bialystok, 2013. - 121 s.
2. Орлов, В.А. Озонирование воды / В.А. Орлов - М.; Стройиздат, 1984. - 88 с.
3. Battino R. Oxygen and Ozone / Battino R. // IUPAC Solubility Data Series. - 1981. - Vol. 7.
- P. 40-55.
4. Sonntag Clemens Chemistry of Ozone in Water and Wastewater Treatment: From Basic Principles to Application / Sonntag Clemens, Urs von Gunten. - London: IWA Publishing, 2012. - P. 287
5. Sedlak David L. The Chlorine Dilemma / Sedlak David L., Urs von Gunten // Science : the Int. J. - 2011. - Vol. 331, № 6013. - P. 42-43.
6. Punmia B. C., Kr. Jain Arun, Jain Ashok. Water Supply Engineering. New Delhi: Laxmi Publication (P) Ltd., 1995. - 584 p.
7. Коган В. Б., Фридман В. Н., Кофаров В.В. Справочник по растворимости. - М.: Химия, 1961. - 961 с.
8. Романовский, В.И. Исследование растворимости озона в воде по высоте столба жидкости / В. И. Романовский, В. В. Лихавицкий, А. Д. Гуринович // Труды БГТУ. - 2015 - № 3 (176): Химия и технология неорган. в-в. - C. 113-118.
9. Disinfection Profiling and Benchmarking Guidance Manual EPA 815-R-99-013. - Published 08.1999. - USA: United States Environmental Protection Agency, 1999. - P. 28.
10. Gurol M. D. Kinetic of. Ozone Decomposition: a Dynamic Approach / Gurol
M. D., Singer P. C. // Environ. Sci. and Technol. - 1982. - Vol. 16, № 7. - P. 377 - 383.
11. Б.Г. Ершов Кинетические закономерности разложения озона в воде / Б.Г. Ершов и [др.] // Химия и технология воды - 2009. - Т. 31, № 6. - 665-676 c.
12. Staehell J. Decomposition of Ozone in Water in the Presence of Organic Solutes Acting as Promoters and Inhibitors of Radical Chain Reactions / Staehelld J., Hoigne J.// Environ. Sci. Technol. - 1985. - Vol. 19. - P. 1206-1213.
13. Леванов А. В. Растворимость и кинетика гибели озона в водных растворах фосфорной и соляной кислоты / Леванов А. В. и [др.] // Вест. Моск. университета. Серия 2 Химия. - 2002. - Т.3 - №5. - 286-287 c.
14. Olah G.A. Oxyfunctionalization of hydrocarbons. 3. Superacid catalyzed oxygena- tion of alkanes with ozone involving protonated ozone, O3H+ / G.A. Olah, N. Yoneda, D.G. Parker // J. Am. Chem. Soc. - 1976. - Vol. 98. - P. 5261-5268.
15. Yoneda N. Oxyfunctionalization of Hydrocarbons, 71a Oxygenation of 2,2- Dimethylpropane and 2,2,3,3- Tetramethylbutane with Ozone or Hydrogen Peroxide in Superacid Media / Yoneda N., Olah G.A. // J.Am.Chem.Soc. - 1977. - Vol. 99. - P. 3113-3119.
16. Yoneda N. Superacid catalyzed oxygena tion of aliphatic ethers with ozone / Yoneda N. [et al.] // Chem. Lett. - 1984. - Vol. 9. - P. 1617- 1618.
17. Jacquesy, J.-C. Functionalisation of non- activated bonds in superacidic media / J.-C. Jacquesy, M.-P. Jouannetaud, A. Martin // Bull. Soc. Chim. Fr. - 1997. - Vol. 134. - P. 425-438.
18. Hoigne J. Rate constants of reactions of ozone with organic and inorganic compounds in water. II: dissociating organic compounds / Hoigne J., Bader H. // Water Research. - 1983. - Vol. 17. - P. 185-194.
19. Разумовский, С.Д. Озон и его реакции с органическими соединениями (кинетика и механизм) / С.Д. Разумовский, Г.Е. Заиков. М.: Наука, 1974. - 322 с.
20. Hoffman S. The urban ozone monitoring by the DOAS technique application / S. Hoffman, W. Sulkowski, K. Krzyzanowski // Molecule Structure - 1995 - Vol. 348, - P. 187- 190.
21. Романовский, В.И. Определение основных параметров дезинфекции и обеззараживания озоном сооружений питьевого водоснабжения / В. И. Романовский, В. В. Лихавицкий, М. В. Рымовская, А. Д. Гуринович // Труды БГТУ. - 2015 - № 3 (176): Химия и технология неорган. в-в. - C. 108-112.
21. Романовский, В.И. Коррозионная устойчивость стали 15 к дезинфицирующим растворам / В. И. Романовский, В. В. Жилинский // Труды БГТУ. - 2015 - № 3 (176): Химия и технология неорган. в-в. - C. 29-34.
22. Романовский, В.И. Коррозионная устойчивость углеродистых сталей к дезинфицирующим растворам / В. И. Романовский, Ю. Н. Чайка // Труды БГТУ. - 2014 - № 3 (167): Химия и технология неорган. в-в. - C. 47-50.
23. Романовский, В.И. Сравнительный анализ эффективности дезинфекции сооружений водоснабжения дезинфицирующими растворами / В.И. Романовский, И.В. Рымовская, С. Янь Фэн // Вода Мagazine. - 2015. - №10(98). - С. 18-21.
24. Романовский В.И. Сравнительный анализ способов дезинфекции водозаборных скважин и сооружений водоснабжения / В.И. Романовский, Ю.Н. Бессонова // Перспективы развития и организационно-экономические проблемы управления производством: мат. межд. научно-технической конференции в 2 томах. Т 1. / Белорусский национальный технический университет. - Минск: Право и экономика, 2015. - С. 211-226.
25. Управление окружающей средой. Оценка жизненного цикла. Применение СТБ ISO 14041-2001 для инвентаризационного анализа жизненного цикла : СТБ ISO/ТО 14049-2007. - Введ. 01.10.2007. - Минск : Гос. комитет по стандартизации, 2007. - 44 с.
Technical aspects of the ozone use for water treatment
The article presents the results of a comparative analysis of the use of ozone and chlorincontaining agents in the processes of water treatment on the following aspects of the use: patterns of dissolved ozone in water, the effectiveness of microorganisms inactivation, corrosion activity, environmental impact assessment on the life cycle stages and life cycle cost assessment.
Keywords: water treatment, corrosion, solubility, disinfection, active chlorine, ozone
Ramanouski Valiantsin Ivanavich, Ph.D. (Engineering), senior lecturer, Department of Industrial Ecology, Belarusian State Technological University (13a, Sverdlova str., 220050, Minsk, Republic of Belarus). E-mail: Адрес электронной почты защищен от спам-ботов. Для просмотра адреса в вашем браузере должен быть включен Javascript.
Hurynovich Anatoli Dmitrievich, Dr. (Engineering), professor, professor, Department of Construction Economics. Belarusian National Technical University (65, Nezavisimosty av., 220013, Minsk, Republic of Belarus). E-mail: Адрес электронной почты защищен от спам-ботов. Для просмотра адреса в вашем браузере должен быть включен Javascript.
Biassonava Yuliya Mikalaeyna, Acting head of regulation and energy saving section, State Enterprise «Minrayteploset'» (134, Sovetskaya str., Zaslavl' town, 223034, Minsk region, Republic of Belarus). Е-mail: Адрес электронной почты защищен от спам-ботов. Для просмотра адреса в вашем браузере должен быть включен Javascript.
Kryshylovich Alena Uladzimiravna, Ph.D. (Chemistry), lecturer, Department of General and Inorganic Chamistry, Belarusian State Technological University (13a, Sverdlova str., 220050, Minsk, Republic of Belarus). E-mail: Адрес электронной почты защищен от спам-ботов. Для просмотра адреса в вашем браузере должен быть включен Javascript.
Журнал «Вода Magazine», №2 (102), 2016 г.
