Основными интегральными показателями загрязненности природных вод органическими веществами являются цветность, перманганатная окисляемость и частично мутность природных вод. Цветность, как известно, определяется в основном присутствием гумусовых кислот, которые условно делятся на гуминовые и фульвокислоты, что объясняется различием их характеристик (таблица 1) [1-2].

Гумусовые кислоты являются многофункциональными высокомолекулярными полидисперсными полимерами природного происхождения. В природе они выполняют различные функции: аккумулирующую, транспортную, защитную, физиологическую. Благодаря наличию и преимущественному содержанию карбоксильных групп гумусовые кислоты изменяют кислотно-основные и окислительно-восстановительные характеристики воды, активно участвуют в процессах комплексообразования с ионами различных металлов, ионогенными органическими веществами. Как следует из таблицы, гуминовые и фульвокислоты, несмотря на сходство, отличаются по элементному составу, растворимости и молекулярной массе. Более окисленная форма фульвокислот при одной и той же концентрации с гуминовыми кислотами характеризуется большей растворимостью, меньшими величинами цветности и перманганатной окисляемости (ПО), чем гуминовые кислоты. Вследствие этого при нормируемых величинах цветности и ПО содержание фульвокислот в воде будет значительно выше, чем гуминовых кислот. Так, нормируемая цветность в 20 град соответствует концентрации фульвокислот в воде, равной 6,5 мг/л (2,9 мг/л ПО), что значительно больше, чем содержание гуминовых кислот - 1,6 мг/л (1,3 мг/л ПО).
Сопоставление ПО гуминовых и фульвокислот показывает, что ПО на 58% может быть обусловлена присутствием фульвокислот и на 26% - гуминовыми кислотами. Остальная часть определяется бесцветной органикой, содержащейся в воде. Различие в свойствах гумусовых кислот определяет и преимущественное присутствие в поверхностных водах фульвокислот, концентрация которых на порядок выше, чем гуминовых кислот [3], и которые, как показано выше, содержатся в значительно больших количествах и в очищенной воде при нормируемых величинах цветности и ПО.
Нормируемый показатель мутности воды, также являющийся интегральным показателем, определяет присутствие в очищаемой воде коллоидных минеральных и органических веществ природного происхождения. К органическим нерастворимым веществам природного происхождения относятся гуминовые кислоты и их нерастворимые соли с ионами тяжелых металлов (железа и др.), а также бактерии и вирусы. Поэтому удаление мутности сопровождается уменьшением содержания не только минеральных веществ, но и коллоидных органических веществ, тяжелых металлов в виде комплексов, уменьшением бактериальной загрязненности. Так, по данным таблицы 1, при мутности очищенной воды, определяемой коллоидными формами гуминовых кислот, в 1,5 мг/л величина ПО составит 1,2 мг/л. Кроме того, известно [4], что снижение мутности водопроводной воды с 1 до 0,5 мг/л сопровождается снижением числа заболеваний населения вирусным гепатитом в 5 раз, а до 0,2 мг/л - в 10-12 раз.
Таким образом, в нормативно очищенной воде присутствуют достаточно высокие концентрации гумусовых кислот, способных образовывать хлорорганические соединения в процессе ее обеззараживания перед подачей воды потребителям, что диктует необходимость применения методов и технологий, которые обеспечивали бы более глубокую очистку воды по мутности, цветности и перманганатной окисляемости.
Существующие способы и схемы очистки поверхностных природных вод, которые включают предварительное хлорирование, коагуляцию, отстаивание, фильтрование и обеззараживание воды, при гарантированном качестве очищенной воды по общим показателям не исключают вторичное загрязнение воды ионами алюминия, железа, хлорсодержащими соединениями, особенно при очистке цветных маломутных вод.
Как известно, изначально первичное хлорирование было предназначено для предотвращения микробного загрязнения и биобрастания очистных сооружений, окисления органических загрязнений и снижения вследствие этого расхода коагулянта при очистке цветных вод. Однако одновременное образование хлорорганических веществ, не удаляемых в процессе двухступенной очистки воды и обладающих канцерогенной и мутагенной активностью, практически полностью нивелируют положительный эффект от применения первичного хлорирования воды. Прежде всего, образуются галометаны, относящиеся к веществам 2-го класса опасности: хлороформ (ПДК = (100 мкг/л), четыреххлористый углерод (ПДК = 6 мкг/л). По результатам работы [5] в процессе хлорирования воды также могут образовываться хлорзамещенные фенолы. При 15 мин. кипячении такой воды содержание фенолов возрастает в среднем в 3,5 раза, 2-хлорфенола - в 2 раза, 2,6 дихлорфенола - в 1,5 раза.
При этом следует отметить, что образование хлорорганических веществ происходит в процессе всего очистного процесса и продолжается в очищенной воде благодаря наличию остаточного хлора в воде после хлорирования. По данным Журбы [6], концентрация хророформа в воде после вторичного хлорирования хотя и меньше нормы, но достаточно высокая, и в зависимости от источника водоснабжения колеблется в пределах от 20 до 85 мкг/л. Содержание четыреххлористого углерода в очищенной воде составляет от 0,2 до 80 мкг/л. При хлорировании воды ионы тяжелых металлов (Cu 2+, Pb 2+ и т. д.) также могут переходить в устойчивые хлоркомплексы (CuCl 2-, PbCl 2-), которые не извлекаются из воды при коагулировании и не удерживаются песчаными фильтрами. Особенно это характерно для железа, марганца, кобальта, свинца, цинка, меди, кадмия [7].
В этой связи самым простым способом предотвращения образования в воде токсичных хлорорганических загрязнений является отказ от первичного хлорирования природных вод, характеризующихся высокой цветностью и ПО, а хлорирование воды использовать только для периодической санации очистного оборудования один раз в полгода или год. Предварительное хлорирование природных вод с высокой концентрацией гуминовых веществ уже запрещено в США и во многих государствах Европы [7].
Вторым способом исключения или уменьшения образования хлорорганических веществ в процессе предварительного обеззараживания воды является применение других обеззараживающих средств: озона, перманганата калия, УФ-облучения, порошкового активированного угля, феррата натрия, бактерицидных органических коагулянтов [6-7], которые могут использоваться самостоятельно и в комбинации друг с другом. В таблице 2 дана сравнительная качественная оценка их обеззараживающей, окислительной и адсорбционной эффективности.
В настоящее время данные способы предварительного обеззараживания воды применяются или прошли промышленную апробацию на ряде водопроводных очистных станциях г. Москвы, Самары, Тольятти и др. городов [8-11]. Например, есть успешный опыт применения УФ-облучения в Самаре для обработки сырой речной воды с цветностью 37-52 град, мутностью 1,2-5,7 мг/л и ПО 6,9-10 мг/л. Коэффициент УФ-пропускания речной воды составил 40-61% [8].
На московских станциях водоподготовки при предварительной обработке воды применяют озон, перманганат калия, порошкообразный уголь [9-10]. При озонировании воды одновременно с обеззараживанием происходит дезодорация воды и снижение цветности. Доза озона в 1 мг/л снижает цветность в среднем на 10 град ХКШ [10]. Применение порошкообразного угля дозами 3-10 мг/л способствует удалению из воды органических веществ, придающих ей запахи и привкусы.
По мнению авторов работы [7], экономически выгодно и эффективно применение феррата натрия Na2FeO4, который по окислительной способности превосходит перекись водорода. Поскольку при его использовании образуется гидроксид железа, он обладает и коагулирующей активностью, что позволяет отказаться от обработки воды минеральным коагулянтом.
Исследованиями, представленными в работе [12], установлено, что органический коагулянт полигексаметиленгуанидин гидрохлорид (ПГМГ) с торговыми названиями «Биопаг», «Полисепт», «Метацид», обладающий биоцидными и коагулирующими свойствами, может служить бесхлорным реагентом комплексного неокислительного действия, одним из альтернативных хлору реагентов в процессах подготовки питьевой воды.
Если отказ от применения хлорсодержащих обеззараживающих агентов на стадии предварительного обеззараживания воды невозможен, технологическая схема очистки цветных вод воды для хозяйственно-питьевого водоснабжения должна дополняться адсорбционными, мембранными и другими методами доочистки от хлорсодержащих и других органических веществ. Одновременно происходит улучшение качества воды по общим показателям: цветности, мутности, ПО [9-11]. Такие схемы реализованы, например, на Юго-Западной и Рублевской станциях водоподготовки г. Москвы. Дооборудование очистных сооружений после отстойника озоносорбцией (озонирование, фильтрование через песчаный и угольный фильтр) на Рублевских очистных сооружениях водоблока №4 позволило получить питьевую воду принципиально другого качества по органическим и хлорорганическим загрязнениям [11]. Так, если цветность очищенной воды по традиционной технологии была не более 12 град, то после озоносорбции - не более 5 град, что соответствовало величинам ПО не более 4 и 2,5 мг/л. На Юго-Западной очистной станции после озонирования осуществляется двухступенчатое углевание воды с фильтрованием воды на двухслойном фильтре на первой ступени и фильтрованием сначала на микрофильтре, затем на фильтре с ультрафильтрационными мембранными модулями на второй ступени. В результате вода полностью очищается от микроорганизмов и растворенных органических соединений [9].
Технология CRISTAL, ультрафильтрация с предварительной обработкой воды порошковым углем в дозе 10-20 мг/л реализована на станции производительностью до 110 тыс м3/сут. во Франции при очистке озерной воды мутностью до 50 мг/л и цветностью до 20 град. Очищенная вода имеет цветность менее 5 град и мутность менее 0,1 мг/л. При этом достигается 100% удаление водорослей, бактерий, кист и вирусов, что было бы невозможно на обычных сооружениях. В технологии используются волоконные мембраны из триацетат-целлюлозы с диаметром пор 1 мм и порогом забиваемости 0,01 мкм, что соответствует отсечению по молярной массе от 100 тыс. до 300 тыс. Дальтон [13].
Самостоятельное применение ультрафильтрации эффективно для очистки и доочистки мутных бесцветных вод. Ультрафильтрационные мембраны с размером пор 0,015- 0,025 мкм, которые задерживают преимущественно коллоидные формы органических минеральных веществ и микроорганизмов, обеспечивают высокий эффект очистки по мутности и снижают бактериальную загрязненность воды. Подтверждением являются результаты, полученные при очистке воды р. Амур, имеющей мутность 64 мг/л, цветность - 50 град, ПО - 7 мг/л, содержание ионов железа - 2,2 мг/л, по схеме: хлорирование, коагуляция с использованием оксихлорида алюминия, отстаивание и ультрафильтрация [14]. Данная схема позволила снизить мутность, содержание остаточного алюминия и железа практически на 100%, цветность - на 55%, ПО - на 68%. Микробиологический анализ очищенной воды показал, что общее микробное число (ОМЧ) было близко к нулю, а общие колиформные (ОКБ) и термотолерантные колиформные (ТКБ) бактерии, колифаги и клостридии отсутствовали. Сравнительно низкий эффект по цветности и ПО свидетельствует о наличии в воде низкомолекулярных органических веществ в растворенном состоянии, которые не задерживаются ультрафильтрационной мембраной с отсечением по молекулярной массе 100 кД.
Ультрафильтрационная технология без предварительной очистки была опробована в НИИ ВОДГЕО при очистке маломутных вод Москва-реки [15]. Для проведения экспериментов использовался отечественный рулонный элемент с ультрафильтрационными мембранами УАМ-150 на основе ацетата целлюлозы с размером пор 0,015 мкм, (что соответствует отсечению по молекулярной массе около 30 000 Дальтон). Вода пропускалась со скоростью 3 м/сек. при давлении 1,5 атм. В результате мутность воды была снижена в 11 раз, содержание фосфатов снизилось в 7 раз, нитритов и аммония - в 2 раза, содержание железа - в 7 раз. Эффективность очистки природной воды от органических веществ составила 25%.
Микро- и ультрафильтрация с предварительной обработкой воды современными коагулянтами и флокулянтами может заменить двухступенчатые схемы очистки природных вод отстаиванием и фильтрованием через минеральные загрузки. Это позволит сократить капитальные и эксплуатационные затраты в 2-3 раза, повысит надежность работы очистных сооружений при одновременном получении очищенной воды стабильного и нормативного качества независимо от колебаний температуры и характеристик очищаемой воды по сезонам года. Так, применение коагулянтов повышает эффективность очистки природной воды от органических веществ ультрафильтрацией с 25% до 60%.
Рассмотренные методы доочистки и повышения качества воды по общим показателям, мутности, цветности, ПО и хлорорганическим веществам, требуют модернизации очистных сооружений и дополнительных капитальных и эксплуатационных затрат. Поэтому самым доступным альтернативным способом повышения эффективности очистки воды по общим интегральным показателям является оптимизация технологии коагуляционной очистки воды на действующих очистных сооружениях путем использования более эффективных коагулянтов и флокулянтов и совершенствования технологического режима их введения. Наличие большого ассортимента коагулянтов и флокулянтов, отдельные из которых обладают бактерицидными свойствами, является положительным фактором для использования данного способа снижения общих физико-химических и микробиологических показателей качества воды.
Как известно, удаление растворенных гумусовых кислот при коагуляционной очистке воды происходит в результате двух процессов:
- сорбции гумусовых кислот на поверхности нерастворимых гидроксидов, образующихся в процессе гидролиза солей алюминия по реакциям:
Al 2 (SO 4 )3 + 3H 2 O ↔ 2Al (OH) 3 ↓ + 3Н 2 (SO 4 )
Al (OH) 2 Cl + H 2 O ↔ Al (OH) 3 ↓ + НС1
- химического взаимодействия гумусовых кислот с ионами алюминия и поликатионами органических коагулянтов с образованием комплексных соединений по реакциям:
6ГумСООН + Al 2 (SO 4 ) 3 ↔
2(ГумСОО ) 3 Аl + 3Н 2 (SO 4 )
ГумСООН + ПолиN + Cl- ↔
Гум СОО- N + Поли + НCl
Данные процессы и определяют способы оптимизации коагуляционной очистки воды [16], к которым относятся (таблица 3):
- выбор эффективного коагулянта и его дозы;
- корректировка щелочности воды;
- применение катионного или анионного флокулянта для укрупнения хлопьев и увеличения эффективности осветления;
- оптимизация гидродинамические условий коагуляции.
Сравнение эффективности разных марок коагулянтов в одинаковых условиях коагуляционной очистки, проведенное на модельных и речных водах (рис.1-7), подтверждает влияние вида применяемого коагулянта и его дозы на степень очистки воды различных водоисточников.
Характеристики исследованных модельных и речных вод представлены в таблице 4. Были исследованы цветные маломутные воды с различной щелочностью (Волга, Орша, Вологда) и мутные воды с низкой цветностью (р. Дон и Кубань).
Влияние вида коагулянта при очистке модельных вод, цветность которых обусловлена гуминовыми или фульвокислотами, показано на рис.1.
Как следует из представленных данных, неорганический коагулянт оксихлорид алюминия (ОХА) лучше снижает цветность воды, чем органический коагулянт ПГМГ, за счет дополнительной адсорбции гумусовых кислот продуктами гидролиза коагулянта. Дозы обоих коагулянтов выше для воды, содержащей фульвокислоты, чем для воды, содержащей гуминовые кислоты при одной и той же исходной цветности воды, что обусловлено более высокой концентрацией фульвокислот в воде.
Влияние вида реагента на эффективность снижения цветности речной воды наглядно иллюстрируют рис. 2-4. Самая низкая цветность отстоянной воды р. Орша достигается при использовании «Полисепта» (ПГМГ) и ОХА. При использовании органических коагулянтов марок ВПК402 и «Каустамин» цветность очищенной воды увеличивается в 2-2,5 раза (рис. 2).

Как следует из рис. 3-4, самой высокой эффективностью при очистке цветных вод р. Волги и Орши обладает более высокомолекулярный «Аква-Аурат» 30 (АА30) и композиционный коагулянт «АкваАурат» 105 (АА105).

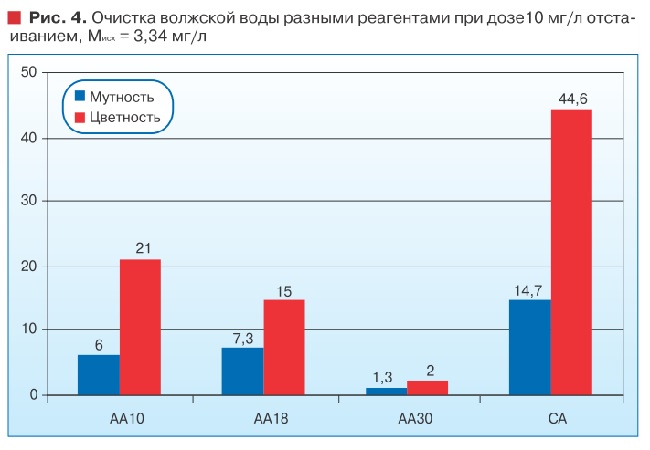
Цветность воды снижается до 2 град, мутность - до 0,71,3 мг/л. Доза коагулянта возрастает с 10 до 25 мг/л при увеличением цветности исходной воды с 85 до 288 град. При высокой щелочности исходной воды, характерной для р. Вологда, несмотря на ее невысокую цветность, доза коагулянта возрастает в 2-3 раза по сравнению с дозой, необходимой для очистки воды с низкой щелочностью, поскольку часть коагулянта расходуется на компенсацию щелочности исходной воды (рис. 5).

Эффект снижения мутности уменьшается за счет выделения углекислого газа, препятствующего осаждению образующихся в процессе коагуляции хлопьев и высокой их концентрации. Максимальное снижение мутности и цветности с одновременным уменьшением дозы сернокислого алюминия, наблюдается при исходной щелочности очищаемой воды от 1,1 до 2,8 мгэкв/л.
Уменьшение исходной цветности ниже нормативной величины (р. Дон и Кубань) влияет не только на выбор ре агента, но и на его оптимальную дозу (рис. 6, 7).

Как видно из рис. 6, для очистки маломутной малоцветной воды р. Дон большей эффективностью для снижения мутности обладает органический коагулянт ВПК 402 самостоятельно либо в сочетании с коагулянтом. Кубанская мутная вода (рис. 7) также лучше очищается с применением органического коагулянта ВПК 402 самостоятельно или совместно с коагулянтом «АкваАурат» 10 (АА10). Причем дозы коагулянтов на два порядка ниже, чем при очистке цветных вод, и составляют 0,1-0,8 мг/л.
Дополнительная обработка воды высокомолекулярным флокулянтом марки «Праестол» (Пр) независимо от его заряда повышает эффект очистки воды отстаиванием по мутности и практически не влияет на эффективность снижения цветности.
Однако, как следует из результатов работ [17-18], содержание остаточного алюминия в очищенных цветных водах снижается больше при использовании катионных, чем анионных или неионных флокулянтов. Этот факт является косвенным доказательством того, что при коагуляции ионы алюминия вероятно образуют с гумусовыми кислотами отрицательно заряженные комплексы, способные осаждаться противоположно заряженными катионными флокулянтами. Соблюдение оптимальных параметров смешения и хлопьеобразования при использовании коагулянтов приводит к снижению мутности в большей степени, чем к уменьшению цветности очищенной воды (рис. 9).
Остаточная мутность может быть уменьшена в 2 раза при увеличении продолжительности хлопьеобразования - с 6 до 10 мин. Цветность очищенной воды при этом меняется незначительно.
Влияние продолжительности смешения коагулянта с очищаемой водой на эффективность очистки воды подтверждается опытом эксплуатации станций водоподготовки при очистке мутных вод р. Дон и Кубань, на которых коагулянты дозируется на водозаборе, что увеличивает длительность перемешивания реагента с очищаемой водой непосредственно в подающем трубопроводе и соответственно возрастает эффективность очистки воды [19].
Оптимизация процесса коагуляционной очистки воды рассмотренными способами позволяет получить очищенную воду с показателями, которые значительно ниже установленных норм, что иллюстрируется данными таблицы 5, где показана цветность и мутность отстоянной речной воды разных водоисточников в оптимальных условиях коагуляции.
Литература:
1. Орлов Д.С. Гуминовые вещества в биосфере // Соровский образовательный журнал. - 1997. - №2. - С.56.
2. Перминова И.В. Анализ, классификация и прогноз свойств гумусовых кислот. Автореф. док. дисс. М., 2000.- 50 с.
3. Лапин И.А., Красюков В.П. Содержание гуминовых и фульвокислот в поверхностных водах СССР. Водные ресурсы / 1991. - 3.- С. 1213.
4. Айдинов Г.Т., Соловьев М.Ю., Зыкова Т.А., Говорухина М.В., Михеева И.В., Гордеев-Гаврилов В.К., Педашенко Д.Д., Божко Л.Н. Снижение мутности питьевой воды как фактор повышения барьерной роли водоочистных сооружений по отношению вирусных загрязнений // Гигиена и санитария. - 2005. - №3. - С.55.
5. Груздев И.В., Кондратенок Б.М., Сталюгин В.В. Гумусовые вещества - источник фенольных соединений в природных и питьевых водах // Международный контактный форум по сохранению местообитаний в Баренцовом регионе: Материалы 4 Совещания, Сыктывкар, 19-25 сентября, 2005. Сыктывкар: Изд-во Коми НЦ УРО РАН, 2006. - С. 56, 311.
6. Классификаторы технологий очистки природных вод. Под ред. Журбы М.Г. НИИ ВОДГЕО. М. - 2000. - 56 с.
7. Скоробогатов Г.А., Калинин А.И. Не пейте сырую воду! Кипяченую тоже, а особенно - водопроводную! (Способы очистки воды в домашних условиях.). НИИХимии СПГУ, Санкт-Петербург. - 2000. - 63 с.
8. Кирсанов А.А., Колчев В.Н., Быкова П.Г., Зайцева С.Г. Внедрение технологии УФ-обеззараживания на предприятиях коммунального хозяйства г. Самары. ВСТ// Водоснабжение и санитарная техника. - 2006. - № 9, ч. 2. - С.25.
9. Храменков С.В., Поршнев В.Н., Привен Е.М. Система водоснабжения Москвы: современное состояние и перспективы развития. ВСТ - 2007. - № 7, ч.1. - С.29.
10. Коверга А.В., Нужный В.Н., Алексеенков С.А., Доможаков Д.И. Качество воды Волжского водоисточника и особенности водоподготовки. ВСТ - 2007. - № 7, ч. 1. - С.35.
11. Шемякин Ю.В., Бабаев А.В., Климова Н.Н. Опыт эксплуатации блока №4 Рублевской станции водоподготовки.- ВСТ - 2006. - № 11, ч.1. - С.13.
12. Ефимов К.М., Гембицкий П.А., Дюмиева И.В., Данилина Н.И. Дезинфицирующие флокулянты для очистки и обеззараживания питьевых и сточных вод. - ВСТ - 2001. - № 6.- С. 13.
13. Моль Жак. Подготовка питьевой воды в 21 веке. ВСТ - 1999.- № 11.- с.2.
14. Домнин К.В., Архипова Е.Е., Самчук И.С., Алешко Д.С., Дунаевская Е.В., Смирнов А.Д., Герасимов М.М., Беляк А.А. Новые технологии очистки воды р. Амура от антропогенных загрязнений. ВСТ - 2007. - № 6, ч.2. - С.32.
15. Первов А.Г., Дудкин Е.В., Мотовилова Н.Б., Андрианов А.П. Ультрафильтрация - технология будущего. ВСТ - 2001. - № 11.- с.9.
16. Гетманцев С.В. Система выбора эффективных технологий очистки природных вод с применением алюмосодержащих коагулянтов. ВСТ - 2011. - № 8. - с.4.
17. Рафф П.А., Селюков А.В., Байкова И.С. Технология контактного осветления воды в условиях Волжского водозабора г. Казани. ВСТ - 2011. - № 6. - с.25.
18. Брусницина Л.А., Пьянков А.А., Богомазов О.А., Лобанов Ф.И., Хартан Ханс- Георг. Опыт применения полиэлектролитов «Праестол» для повышения качества питьевой воды и обезвоживания осадков. Вода и экология. - 2000. - № 1. - с.40.
19. Педашенко Д.Д., Божко Л.Н. Производственные испытания обработки воды реагентами полиДАДМАХ и «Аква-Аурат» 10 для водоснабжения г. Ростова-на- Дону. Технология очистки воды «Техновод-2005»: Материалы научно-практической конференции, Казань, 2005 г.- с.67.
Журнал «Вода Magazine», №1 (65) , 2013 г.
